Utilisation du pericarde autologue
UTILISATION DU PERICARDE AUTOLOGUE TRAITE PAR UN POLYMERE D’HYDROGEL DANS LA RECONSTRUCTION VALVULAIRE AORTIQUE : ETUDE DE FAISABILITE CHEz LE MOUTON
RECONSTRUCTION OF AORTIC VALVE WITH AN AUTOLOGOUS PERICAR-DIUM PRETRAITED WITH A POLYSACCHARIDE GEL: FEASABILITY STUDY IN AN EXPERIMENTAL SHEEP MODEL
MAGUETTE BA1,2 *, ISABELLE DI CENTA3 , NIzAR KHELLIL1 , REMI ESCANDE1 , AICHA
ABED1 , GRACIELA PAVON1 , EMMANUEL LANSAC4 , ANNE MEDDAHI PELLÉ1,2 .
1INSERM U1148 – Laboratoire de Bio-Ingénierie des Polymères Cardiovasculaires (BPC), CHU Xavier
Bichat, 46 rue Henri Huchard, 75018 Paris
2 Institut Galilée, Université Paris 13, 99 avenue J.B Clément, 93430 Villetaneuse
3 Hôpital Foch, 40 rue Worth, 92151 Suresnes
4 Institut Mutualiste Montsouris, 42 Boulevard Jourdan 75014 Paris
Auteur correspondant : Dr Maguette Ba BP 12699 Dakar Colobane
Email : ba.maguette@yahoo.fr
Résumé
Le choix d’une valve de remplacement pose de nombreux pro- blèmes surtout chez l’enfant et l’adulte jeune en raison de la dégénérescence précoce des bioprothèses et des contraintes du traitement anticoagulant. L’utilisation du péricarde du malade pour confectionner une valve de remplacement durant le même temps opératoire serait une alternative intéressante. Elle per- mettrait d’obtenir un substitut valvulaire autologue, disponible à faible coût. Le but de cette étude est de mettre au point et de valider cette technique de reconstruction valvulaire aortique avec le péricarde autologue traité par un hydrogel de polysac- charides dans un modèle expérimental chez le gros animal. Cinq (5) moutons ont été opérés à cœur ouvert sous anesthé- sie générale et circulation extra corporelle. Par thoracotomie postéro-latérale gauche au 4ème espace inter costal gauche, la valve aortique native est réséquée et remplacée par une néo- valve en péricarde autologue prétraitée par le polymère. La néo- valve est implantée grâce à 3 hémi-surjets de Prolène 4/0 selon la technique décrite par Goetz. Les temps moyens de CEC et de clampage aortique sont respectivement de 140 et 79 minutes. Les durées moyennes de fabrication et d’implantation de la valve péricardique sont de 14 et 49 minutes. Il y’avait 2 cas de micro fuite centrale à l’échocardiographie de contrôle. Deux des 5 moutons sont morts sur table par défaillance myo- cardique sévère. L’utilisation du péricarde autologue traité par un hydrogel de polysaccharides dans la reconstruction valvu- laire aortique est une technique faisable avec destemps de pré- paration et d’implantation de la valve acceptables sans détério- ration précoce de la valve. Les résultats histologiques après sacrifice des animaux survivants permettront de mieux évaluer cette méthode de traitement des tissus valvulaires. Mots-clés : Valve aortique, péricarde autologue, hydrogel, étude expérimentale, in vivo.
INTRODUCTION
Les cardiopathies valvulaires rhumatismales consti- tuent un grand défi sanitaire pour les pays sous- développés en raison de leur forte prévalence et des nombreux problèmes que pose leur prise en charge. L’atteinte des valves du cœur est liée dans ce cas à une réponse immunitaire inappropriée secondaire à des angines mal soignées, survenues dans la petite enfance [1, 2 ,3]. Le traitement de ces valvulopathies rhumatismales cardiaques nécessite à terme un remplacement de la valve défectueuse par une prothèse mécanique ou biologique. Ces valves de remplacement posent des problèmes non encore résolus liés à la dégénéres- cence des prothèses biologiques et aux contraintes du traitement anticoagulant qu’imposent les prothèses mécaniques [4, 5, 6]. De plus, le coût onéreux de ces prothèses valvulaires manufacturées constitue un facteur limitant la prise en charge chirurgicale des malades dans les pays pauvres. L’utilisation du péricarde du malade ou autogreffe permettant de confectionner à moindre coût une valve de remplacement dans le même temps opéra- toire, est une alternative intéressante. Le péricarde est, en effet, une membrane séreuse qui entoure le cœur et a des propriétés mécaniques capables de lui conférer les atouts fonctionnels d’une valve de rem- placement [7]. Comme tout tissu bio- prothètique, ce péricarde doit être prétraité avant implantation. Ce prétraitement permet de stabiliser la matrice extra cellulaire qui est ainsi préservée de la dégradation enzymatique. Le glutaraldehyde est le composé de prétraitement dessubstitutstissulaires valvulairesla plus utilisée. Il s’agit d’un dialdéhyde aliphatique capable de se lier aux groupes aminés libres des composants tissulaires comme le collagène et de former des liaisons cova- lentes entre les fibres de collagène (effet tannant) permettant ainsi de stabiliser la matrice extracellu- laire et d’améliorer ses capacités mécaniques [8]. Cependant, le glutaraldéhyde a une certaine cyto- toxicité et il est même incriminé dans la genèse de la dégénérescence des bioprothèses en dévitalisant les cellules de soutien [9]. Différentes stratégies sont explorées à l’heure actuelle afin de mettre au point une méthode de pré- traitement des tissus valvulaires efficace et moins délétère que le glutaraldéhyde [10, 11]. Notre travail s’inscrit dans cette optique en utilisant un hydrogel
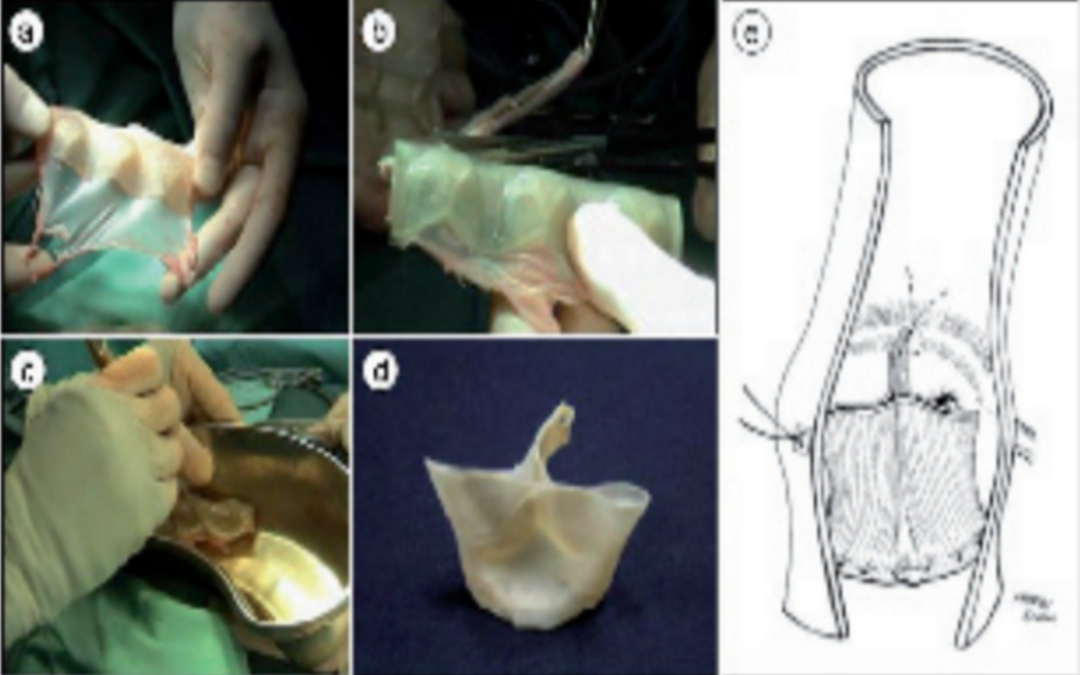
dante par une canule coudée 18 Fr. La canulation veineuse était faite par une canule à double étage atrio-cave de 32Fr. Dès que les canules étaient rac- cordées à l’oxygénateur, la CEC était amorcée en normothermie. L’aorte ascendante était clampée au ras du tronc supra aortique unique. Le cœur était ensuite arrêté par une solution de cardioplégie chaude au sang injectée par la racine aortique puis renouvelée toutes les 20 minutes par les ostia coronaires après l’ouver- ture de l’aorte par une aortotomie transversale réali- sée 1 cm au-dessus de la jonction sino-tubulaire. Confection et implantation de la valve en péricarde traitée par un gel de polymère La valve native était ensuite réséquée et la taille de l’anneau aortique mesurée grâce à des bougies de HEGAR permettant ainsi de choisir le moule corres- pondant à la taille de la valve. La large pièce de péri- carde prélevée était étalée sur le moule correspon- dant à la taille de l’anneau natif puis découpée et confectionnée selon la technique décrite par Goetz [12] (fig.1). La néo-valve péricardique était ensuite fixée par immersion dans une solution contenant le polymère d’hydrogel.Afin de déterminer la composition idéale pour l’application finale, nous avons réalisé plu- sieurs gels polysaccharidiques de compositions dif- férentes en utilisant le dextrane, le pullulane et l’hé- parine (tableau I). L’agent de réticulation utilisé a été le POCl3 (fig.2) permettant une polymérisation rapide du polymère en moins de 5 minutes du fait des contraintes de temps liées à la CEC. Le mélange utilisé était P100D0H. Il autorise une polymérisation rapide en 2 minutes 25 secondes et suffisamment longue pour permettre de recouvrir tout le tissu péricardique. Le tableau II résume les paramètres retenus pour la préparation du gel. La néo- valve en péricarde était ensuite implantée sur l’anneau aortique par 3 hémi-surjets au Prolène 4/0. Les 3 commissures étaient fixées au niveau de la paroi aortique par 3 points en U appuyés sur attelle. L’aortotomie était fermée par 2 hémi-surjets de Prolène 5/0. Après purge des cavités cardiaques, l’aorte était déclampée et le cœur était assisté pendant 20 à 30 minutes en fonction de la tolérance du clampage aor- tique. Evaluation peropératoire et suivi post-opératoire
Lors de la phase de réparation, les cellules des tissus lésés libèrent des produits de l’inflammation tels que les cytokines (Interleukine 1, 6, 10 etc.) et les fac- teurs de croissance (par exemple le Tumor Necrosis Factors ou TNF) chargés de la mobilisation des macrophages pour la détersion de la lésion [17, 18], mais aussi des radicaux oxygénés [19] qui vont accroitre la mortalité cellulaire et aggraver les méca- nismes de fibrose [20]. L’utilisation du péricarde autologue à l’état frais sans prétraitement entraine une détérioration précoce du greffon valvulaire par épaississement du tissu péri- cardique et une incidence élevée d’endocardites post opératoires [14]. Le prétraitement des implants tissu- laires même autologues permet de minimiser le phé- nomène de remodelage tissulaire et de stabiliser leur matrice extra-cellulaire ce qui les préserve d’une possible dégradation enzymatique [9, 21]. Le gluta- raldéhyde est à l’heure actuelle le composé de pré- traitement des biomatériaux valvulaires le plus uti- lisé. Il a cependant une certaine cytotoxicité qui pro- voque une devitalisation des cellules interstitielles qui serait le point de départ du processus de minéra- lisation des tissus bio-prothètiques [9, 21, 22]. De nombreuses autres composés alternatifs sont actuel- lement testées et évaluées. C’est le cas notamment du gel polysaccharidique que nous avons utilisé dans le cadre de ce travail de recherche. Cet hydrogel de polysaccharide serait moins délétère que le glutaral- déhyde dans le prétraitement des tissus bioprothè- tiques [23]. Le recouvrement du péricarde par ce gel de polysac- charides permet de lui conférer une surface compa- tible avec le flux sanguin et de minimiser lesrisques de fibrose rétractile à court terme. Dans cette étude, nous avons sélectionné trois types de polysaccha- rides : le pullulane, le dextrane, et l’héparine. Les deux premiers sont connus pour leurs caractères ioniques en milieu alcalin et par la possibilité éven- tuelle de pouvoir les modifier chimiquement. L’héparine est utilisée dans la composition du gel pour sa capacité à former un « glycocalix » à la sur- face membranaire cellulaire. Lee et al. ont montré qu’en traitant des péricardes decellularisés et tannés au glutaraldéhyde par l’héparine, la matrice résistait mieux à la dégradation enzymatique notamment par la collagénase [24]. L’héparine, appartenant à la famille des héparane -sulfates, est présente dans les cellules mastocytaires des tissus. Elle est connue pour, à la fois protéger les éléments constitutifs de la …
Summary
The choice of valvular substitute poses numerous challenges particular in the children. The use of the patient own pericar- dium for constructing heart valve prosthesis is an interesting alternative and has several potential advantages: there is no immune reaction between the host and the implanted valve and their low cost is an attractive solution for patients in the deve- loping countries. The aim of our study is to focus and evaluate technical aspects of construction and implantation of autolo- gous pericardium prosthesis prétraited with polysaccharide gel. Five (5) sheep underwent aortic valve replacement with autologous pericardium prosthesis according to Goetz’s tech- nique using cardiopulmonary bypass. The heart was exposed with a standard left thoracotomy through the 4th intercostal space. Cardiopulmonary bypass and cross-clamp mean time was 145 min and 79 min respectively. The prosthesis mean time construction and surgical implantation was 14 and 49 min res- pectively. Echocardiograhic study showed trivial central regurgitation in 2 cases. Two sheep died owing myocardial fai- lure at the end of the procedure. Truly stenless aortic valve replacement using autologous pericardium pretraited with a polysaccharide hydrogel is feasible, with cross clamping time acceptable and without precoce structural dégénération. Histological results are particulary useful to evaluate this new method for pericardial valvular implant using polysaccharid gel.
Keywords: Aortic valve, autologous pericardium, hydrogel, experimental study, in vivo.
de polysaccharides pour prétraiter l’autogreffe péri- cardique dans la reconstruction valvulaire aortique. Cet hydrogel permettrait d’augmenter la viabilité et la capacité de recolonisation des tissus. Il s’agit d’une étude de faisabilité dont le but est de mettre au point et d’évaluer les techniques de fabri- cation et d’implantation chirurgicale de la valve en péricarde autologue traitée par un hydrogel de poly- saccharide dans un modèle animal expérimental.
MATERIEL ET METHODES
Toutes les procédures du protocole expérimental ont été réalisées conformément aux recommandations dictées par le guide de soins et d’utilisation des ani- maux de laboratoire (Guide for the Care and Use of Laboratory Animals- National Research Council 1996). Modèle expérimental Cinq (5) moutons de la race «préalpes» ont été opé- rés pour une reconstruction de la valve aortique avec le propre péricarde de l’animal. L’âge moyen des animaux était de 12 mois et le poids moyen de 50 Kg. Les interventions sont faites sous anesthésie géné- rale avec une prémédication à la Kétamine à la dose de 1mg/Kg. Les animaux étaient intubés par voie oro – trachéale et ventilés mécaniquement en mode volume contrôlé (respirateur Drager Primus ®). L’anesthésie était entretenue par l’isoflurane et le propofol. L’électrocardiogramme était monitoré de façon continue grâce à 4 électrodes transcutanées, la satu- ration capillaire était mesurée par un capteur au niveau de l’oreille. Prélèvement et préparation du péricarde Le cœur a été abordé par une large thoracotomie pos- téro-latérale gauche dans le 4ème espace intercostal. La face médiastinale du péricarde a été disséquée et débarrassée des reliquats graisseux pleuraux et thy- miques. Une large pièce rectangulaire de péricarde était ensuite prélevée partant de la ligne médiane jusqu’aux limites du nerf phrénique gauche. La pièce de péricarde était ensuite mise dans une cupule de sérum salé isotonique glacé. Mise en place de la Circulation Extra-corporelle (CEC) La circulation extra-corporelle (CEC) était installée après héparinisation générale à la dose de 300 uni- tés/Kg. L’aorte était canulée au niveau de l’aorte descen-
Après sevrage de la CEC, la qualité du remplace- ment valvulaire aortique était évaluée sur des para- mètres échocardiographiques et hémodynamiques. L’échocardiographie épicardique en coupe petit axe mode 2D avec doppler couleur permettait de recher- cher une fuite valvulaire aortique significative. Sur le plan hémodynamique, on vérifiait la dilatation du ventricule gauche (VG) et le gradient trans-valvu- laire par la mesure du gradient VG – Aorte. Les moutons étaient suivis les six premiers jours post-opératoires aux locaux du laboratoire animalier, puis ils étaient transférés à la ferme dans l’attente de la date prévue de leur sacrifice.
RESULTATS
Le temps de CEC moyen pour toutes les procédures chirurgicales était de 140 min et le temps de clam- page aortique moyen de 79 min. Le temps moyen de confection de l’autogreffe péri- cardique était de 14 min. Le temps moyen de pose de l’autogreffe en position orthotopique sous coronaire était de 49 min. L’échocardiographie per opératoire a montré 2 cas de fuite valvulaire minime centrale sans aucune conséquence hémodynamique. Il n’y a eu ni fuite para-valvulaire ni thrombose valvulaire. Deux moutons sont morts sur table en per procédure. Le sevrage de la CEC avait été dansles 2 casimpos- sible malgré une longue période d’assistance circula- toire. Celle-ci était arrêtée devant un tableau de défaillance myocardique sans qu’on ait pu faire la preuve d’une insuffisance valvulaire aortique majeure.
DISCUSSION
Le concept de fabrication d’une bio-prothèse valvu- laire cardiaque à partir de tissu autologue (fascia lata, péricarde) est aussi ancien que la chirurgie val- vulaire [13, 14]. Le péricarde possède en effet des propriétés biomécaniques et une disponibilité qui en font un substitut tissulaire intéressant [7]. De plus son utilisation comme substitut valvulaire auto- logue n’entraine pas de phénomène de rejet comme c’est le cas pour les xénogreffes. Néanmoins, la présence de débris cellulaires et matriciels va induire un phénomène de remodelage tissulaire [15, 16] qui peut être à l’origine d’une fibrose post-opératoire lors de la phase de réparation. Cette fibrose peut être rétractile et entrainer in fine une insuffisance valvu- laire par défaut de coaptation des feuillets. En effet,
matrice de la dégradation protéasique, mais égale- ment joue un rôle dans la signalisation cellulaire en protégeant lesfacteurs de croissance de type heparin- binding growth contre les dégradations enzyma- tiques type élastase, collagénase ou plasmine pré- sents lors de la réparation, favorisant ainsi la multi- plication cellulaire et la réparation tissulaire [25]. De plus, elle assure une protection contre la dégradation par les radicaux libres [26]. Le choix de l’agent réticulant s’est porté sur le POCl3 au lieu du Sodium Trimétaphosphate (STMP) qui est plus biocompatible et plus souvent utilisé [23]. Le STMP ne pouvait pas être utilisé dans cette étude car le temps de réticulation est trop long (10 à 15 minutes) par rapport au cahier des charges. Nous avons cependant ajusté la concentration de l’agent réticulant (POCL3) et choisi un mélange de pullulane hépariné qui mettait environ 2 minutes à former un gel (tableau II). Cette composition a été retenue car compatible avec le cahier des charges qui impose un temps moyen de confection de la valve à 15 min environ. Les résultats immédiats de ce travail montrent qu’il est possible d’utiliser le péricarde autologue pré- traité par un gel de polysaccharides dans la recons- truction valvulaire aortique sans risque de dégrada- tion enzymatique ni de fibrose précoce du tissu val- vulaire. De même les observations réalisées tant en per-opératoire, qu’en post-opératoire immédiat n’ont pas mis en évidence de thrombus à la surface de la valve péricardique.Apressacrifice des animaux survivants (12 mois après l’intervention chirurgi- cale), les résultats des examens macroscopiques et histologiques des valves explantées permettront d’évaluer cette méthode de prétraitement des tissus valvulaires par rapport au glutaraldéhyde qui est la référence. Sur le plan de la technique chirurgicale, les princi- pales difficultés rencontrées au cours des procédures étaient liées à l’absence de stent et de collerette de suture de l’autogreffe péricardique. Le recouvre- ment par l’hydrogel ne permettait pas de rigidifier suffisamment le tissu péricardique qui devait être déplissé à chaque point de passage du surjet. En pre- nant en compte ces difficultés opératoires, il sera utile d’utiliser des instruments dédiés comme un porte – valve adapté qui permettra de simplifier notamment l’implantation chirurgicale. Celle-ci consiste à réaliser un surjet circulaire pour fixer la néo-valve sur l’anneau valvulaire aortique avec trois
(3) points d’attaches commissurales sur la jonction sino-tubulaire capables de résister à des forces axiales engendrées par des pressions supérieures à 200 mm Hg très largement supérieures aux pressions diastoliques chez l’homme [12, 27]. L’absence d’armature de l’autogreffe péricardique ou valve « stentless » permet de maximiser la sur- face utile de la valve, ce qui constitue un réel avan- tage de cette technique de remplacement valvulaire chez les malades qui ont une dysfonction ventricu- laire gauche ou un petit anneau aortique comme c’est le cas chez l’enfant [4, 6]. De plus la suture directe de l’autogreffe valvulaire péricardique sur l’anneau aortique natif ou la paroi de l’aorte permet de préserver l’anatomie fonction- nelle de toute la racine de l’aorte et les capacités de croissance de l’anneau natif [4, 28]. Les contrôles écho-cardiographiques ont montré un bon fonctionnement de l’autogreffe dans tous les cas avec seulement une fuite centrale minime dans deux cas sans aucune conséquence hémodynamique. La mortalité per-opératoire est souvent élevée (envi- ron un animal sur deux) dans ce type de procédures qui sont lourdes nécessitant l’utilisation de la CEC et un arrêt du cœur plus ou moins long. Le mouton est pourtant considéré comme le modèle expérimental de choix en chirurgie valvulaire [29]. D’autres modèles animaux, tels que le bœuf ou le chien, sont également utilisés car ils supportent le sevrage de la CEC. Ils posent néanmoins, pour le premier des pro- blèmes de coûts et d’équipements encore plus lourds et pour le second des problèmes éthiques. Le porc, fréquemment utilisé dansl’évaluation des matériaux, tolèrent très mal le sevrage de la CEC et est sujet à de nombreuses complications post opératoires, notamment des péricardites. Le mouton présente
l’intérêt d’avoir des constantes cardiaques (fré- quence cardiaque, débit cardiaque, pression arté- rielle, gazométrie sanguine, électrocardiogramme) superposables à celles de l’homme [30]. Il en est de même pour la numération et la formule sanguine [31]. Il présente également un métabolisme phos- pho-calcique rapide qui permet d’objectiver rapide- ment les résultats. Les calcifications apparaissent en moyenne vers 6 mois [30]. Il s’agit par ailleurs d’un animal disponible,simple d’élevage et d’entretien. Il est donc considéré comme un bon modèle expéri- mental en chirurgie cardiovasculaire avec des résul- tats satisfaisants et une mortalité péri-opératoire acceptable, à condition que les procédures chirurgi- cales ne nécessitent pas des temps de CEC longs [29]. Le clampage aortique est moins bien supporté dans les procédures longues parce qu’il s’agit de cœurs sains donc sans pré-conditionnement. Les cas de décèssur table dans cette étude seraient liés à une défaillance myocardique probablement due à cette intolérance des animaux à des procédures chirurgi- cales relativement longues sans préconditionne- ment.
CONCLUSION
L’utilisation d’une valve en péricarde autologue pré- traitée par un hydrogel de polysaccharides dans la reconstruction valvulaire aortique est techniquement faisable chez le gros animal sans détérioration pré- coce de la prothèse. L’évaluation à long terme se fera après sacrifice des animaux survivants (12 mois après l’intervention chirurgicale). Les examens macroscopiques et histologiques des valves explan- tées permettront d’évaluer et de comparer cette méthode de prétraitement des tissus valvulaires par rapport au glutaraldéhyde qui est la référence.


Figure 1 : Confection de la néo-valve. (A) Découpe du péricarde à l’aide du moule corres-pondant à la taille de l’anneau natif. (B) Aspect de la néo-valve après implantation en 3D